IHC・ISH試薬 Molecular Diagnostics Division
保管温度2~8℃
用手法用 ヒストステイナー用 ヒストステイナーAT用
MTAPmethylthioadenosine phosphorylase
■動物種:ウサギ
■使用目的:
組織・細胞中のヒトMTAPタンパク質の染色
ホルマリン固定パラフィン包埋切片の免疫染色に使用できる。
研究用としてのみ使用すること。
■資料
リーフレット
スクロールで確認できます→
用手法用
ヒストステイナー用
ヒストステイナーAT用
※弊社へお問い合わせください
特異性および抗原分布
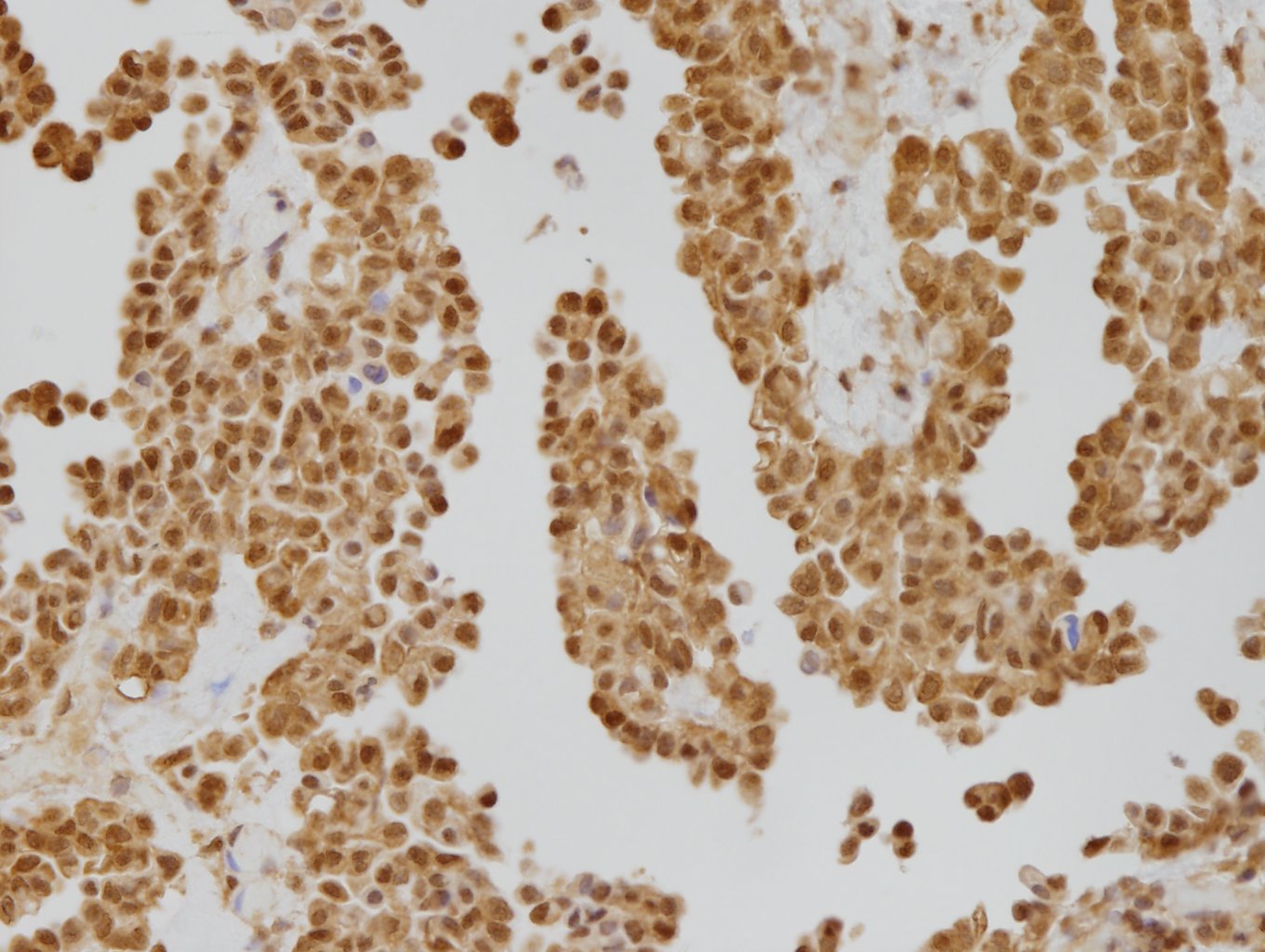
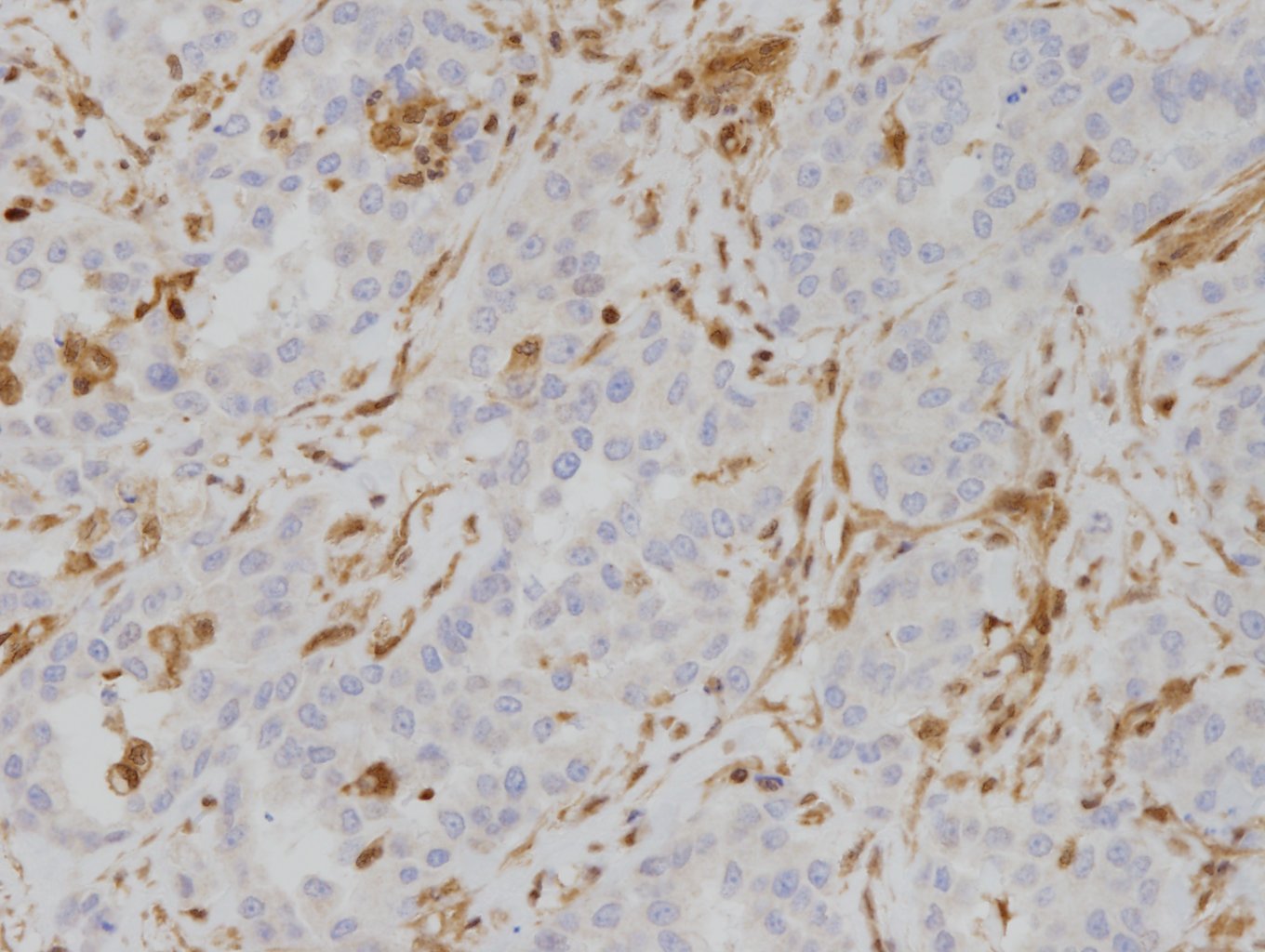
ヒトMTAP(methylthioadenosine phosphorylase)タンパク質と特異的に反応する。MTAPは、ポリアミン合成に伴って生じるMTA(5'-methylthioadenosine)を分解し、アデニンおよびメチオニンのサルベージ経路に関与する酵素である(1)~(4)。MTAP遺伝子はヒト9番染色体の短腕(9p21.3)に位置し、同領域にあるCDKN2A遺伝子と近接している(1)~(4)。両遺伝子は中皮腫などで共欠失するため、MTAPの免疫組織化学染色(IHC)は、Fluorescence in situ ハイブリダイゼーション(FISH)法によるCDKN2Aのホモ接合性欠失検出(CDKN2A FISH)の代替アッセイとして認識されている(2)(5)~(7)。正常では、中皮細胞、平滑筋細胞、尿路上皮細胞など、ほとんどの細胞の細胞質に反応がみられる(3)(6)。腫瘍では、中皮腫(胸膜: 約50%、腹膜: 約5~10%)、膵管腺癌、尿路上皮癌、非小細胞肺癌などで、MTAPの細胞質からの消失(MTAP loss)がみられることがある(1)(4)~(7)。胸膜中皮腫の組織型別では、上皮様中皮腫35%(8)~67%(2)、二相性中皮腫59%(8)、肉腫様中皮腫61%(9)~83%(8)でMTAP lossが報告されている。胸膜中皮腫と反応性中皮過形成の判別において、BAP1 IHC(核からの消失)、MTAP IHC(細胞質からの消失)、CDKN2A FISH(ホモ接合性欠失)による遺伝子異常に基づいた補助的アッセイが有用であると報告されている(2)(3)(5)(10)。
注1: MTAPが発現している細胞では、細胞質の他に核にも染色がみられる場合がある。
注2: MTAP lossを示す細胞では、細胞質の染まりは消失しているが核に染色がみられる場合がある。
注3: MTAP lossの有無を評価する際は、内在性陽性コントロール(内皮細胞、炎症性細胞、線維芽細胞など)が陽性であることを必ずご確認のうえ判別ください(5)(10)。
文献
(1) Fan N,et al. Methylthioadenosine phosphorylase deficiency in tumors: A compelling therapeutic target. Front Cell Dev Biol. 2023 Apr 5;11:1173356.
(2) Berg KB, et al. Utility of Methylthioadenosine Phosphorylase Compared With BAP1 Immunohistochemistry, and CDKN2A and NF2 Fluorescence In Situ Hybridization in Separating Reactive Mesothelial Proliferations From Epithelioid Malignant Mesotheliomas. Arch Pathol Lab Med. 2018 Dec;142(12):1549-1553.
(3) Kinoshita Y, et al. A combination of MTAP and BAP1 immunohistochemistry in pleural effusion cytology for the diagnosis of mesothelioma. Cancer Cytopathol. 2018 Jan;126(1):54-63.
(4) Clouser MC, et al. A systematic literature review of MTAP deletions in solid and hematologic Cancers. Cancer Treat Res Commun. 2025;44:100966.
(5) Husain AN, et al. Guidelines for Pathologic Diagnosis of Mesothelioma: 2023 Update of the Consensus Statement From the International Mesothelioma Interest Group. Arch Pathol Lab Med. 2024 Nov 1;148(11):1251-1271.
(6) Gorbokon N, et al. Prevalence of S-methyl-5'-thioadenosine Phosphorylase (MTAP) Deficiency in Human Cancer: A Tissue Microarray Study on 13,067 Tumors From 149 Different Tumor Types. Am J Surg Pathol. 2024 Oct 1;48(10):1245-1258.
(7) Brune MM, Savic Prince S, et al. MTAP as an emerging biomarker in thoracic malignancies. Lung Cancer. 2024 Nov;197:107963.
(8) Chapel DB, et al. Clinical and molecular validation of BAP1, MTAP, P53, and Merlin immunohistochemistry in diagnosis of pleural mesothelioma. Mod Pathol. 2022 Oct;35(10):1383-1397.
(9) Terra S, et al. Loss of Methylthioadenosine Phosphorylase by Immunohistochemistry Is Common in Pulmonary Sarcomatoid Carcinoma and Sarcomatoid Mesothelioma. Am J Clin Pathol. 2022 Jan 6;157(1):33-39.
(10) 日本石綿・中皮腫学会, 日本肺癌学会[編]. 中皮腫瘍取扱い規約. 第2版. 東京: 金原出版; 2025. 184 p.

食道